跳过内容
长春应化所逯乐慧团队最新JACS:纳米电化学新工具!碳配位钴平台实现脑胶质瘤中神经化学物质的选择性监测
胶质母细胞瘤(GBM)是最致命的原发性脑肿瘤之一,其危害不仅来自占位效应,还因肿瘤细胞弥漫浸润破坏神经网络,导致认知、运动及精神功能衰退。最新研究显示,GBM 细胞甚至可能主动劫持神经信号,促进自身生长,形成肿瘤进展与神经功能恶化的恶性循环。多巴胺(DA)在认知、运动与奖赏调控中起核心作用,其异常可能与 GBM 发展相关,因此原位追踪 DA 动态对理解 GBM 相关神经功能损伤至关重要。然而,现有检测手段受时间或空间分辨率、定量能力及操作复杂度限制;可植入微电极虽具高时空分辨率,但在 GBM 特有的高氧化、酸性、活性物质丰富的微环境中仍面临稳定性和选择性挑战。
近期,中国科学院长春应用化学研究所逯乐慧研究员/刘辰博士和湖南大学刘艳岚教授合作构建了一种碳配位过渡金属钴纳米催化体系(CoCx@C),并将其集成于微电极平台,用于胶质瘤浸润的脑内多巴胺原位选择性电化学监测。相关工作以“Carbon-Coordinated Cobalt Electrochemical Nanoplatform Enables in Vivo Selective Monitoring of Neurochemical Dysregulation in Glioblastoma-Infiltrated Brain”为题发表在Journal of the American Chemical Society.
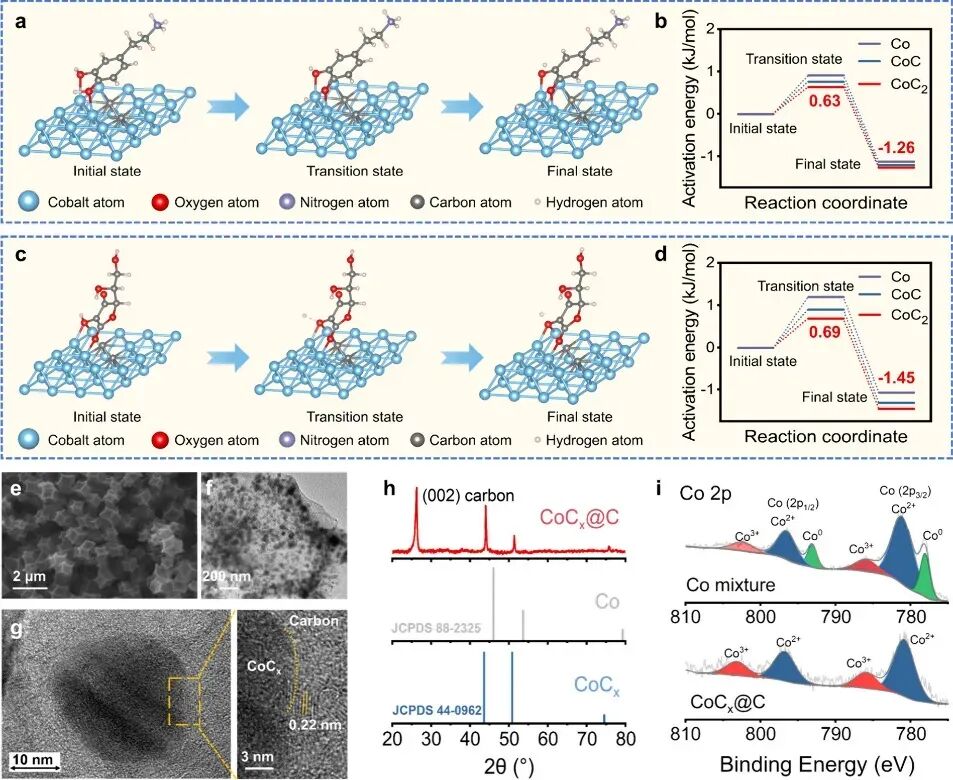
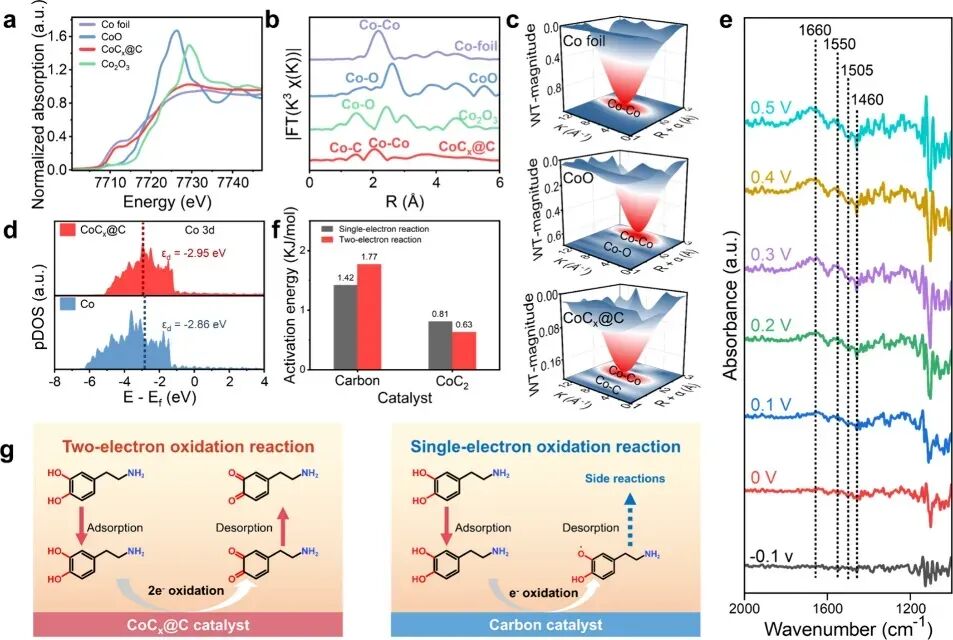
该材料经快速焦耳热处理(2秒内升温至2000℃,随后2秒快速降至室温),制备出碳配位钴纳米催化剂,并形成外层碳壳保护结构,从而赋予电极良好导电性、催化活性及体内稳定性,为神经递质检测提供可靠基础(图1和图2)。
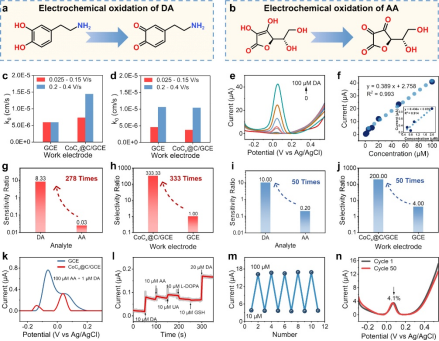
不同于依赖单电子转移过程的碳电极,该体系在碳配位结构调控下,使多巴胺氧化反应沿多电子转移路径进行,促进其向多巴胺醌(DAQ)的转化过程,从而增强电流信号强度与反应动力学效率(图3)。值得一提的是,该纳米结构的外层碳壳为催化剂提供物理保护,不仅减少金属离子流失,也增强了材料在肿瘤高反应性微环境中的生物相容性与稳定性。
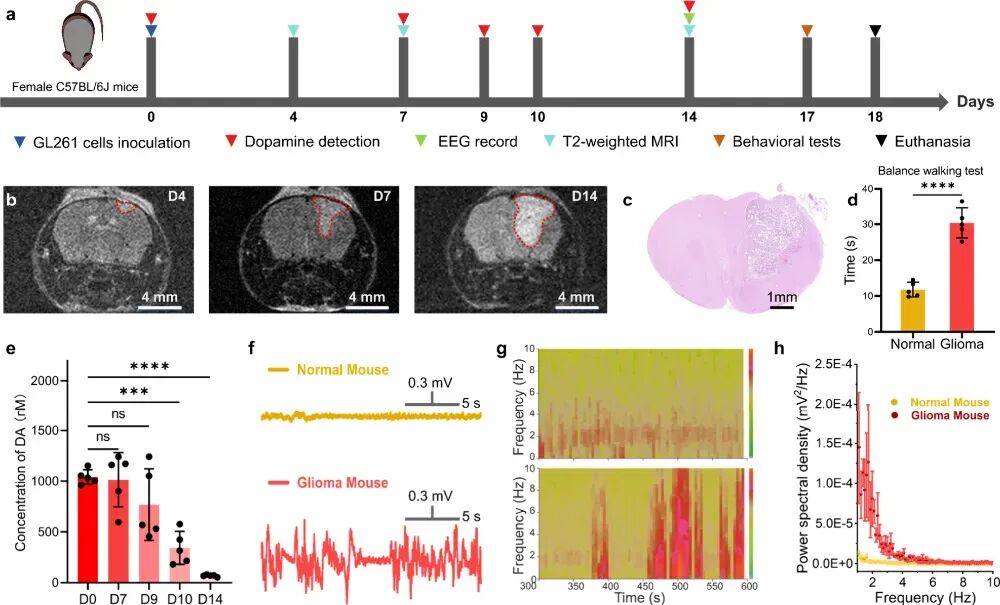
基于CoCx@C微电极平台,研究进一步开展了在体神经化学动态监测探索,实现了对多巴胺的实时追踪。结果显示,在胶质母细胞瘤进展过程中,肿瘤组织会持续扰动多巴胺信号,并且伴随着神经电生理信号的紊乱,提示神经递质稳态失衡可能是肿瘤相关神经功能损伤的重要机制之一(图4)。相关发现为理解肿瘤—神经相互作用提供了直接电化学证据。
该研究构建的碳配位钴纳米电化学平台,实现了在复杂脑肿瘤微环境中对神经递质的高灵敏、高选择性检测,为神经肿瘤学研究提供了一种可用于原位动态监测的工具。随着神经科学与肿瘤学交叉研究的不断深入,这类能够“读出脑内化学语言”的电化学技术平台,或将成为未来神经肿瘤研究与干预的重要支撑工具。
lehuilu2026-04-02T19:21:25+08:00